Traumatisme dans l’enfance et sensibilité au stress à l’âge adulte
Christine Heim, Ph.D.
Emory University, États-Unis
Introduction
Ces dernières décennies, la société a pris de plus en plus conscience de la maltraitance (abus et négligence) des enfants, qui est maintenant considérée comme un problème de santé publique aux proportions épidémiques.1 De plus, un grand nombre d’enfants connaissent la perte d’un parent ou vivent avec un parent atteint de maladie mentale qui est fort probablement incapable de leur assurer des soins assidus ou adéquats. Des données probantes montrent que les traumatismes durant l’enfance constituent un important facteur de risque prédisposant aux troubles de l’humeur et à l’anxiété ainsi qu’à certaines maladies, comme les cardiopathies et les syndromes de fatigue ou de douleur chronique.2 À l’âge adulte, ces désordres fonctionnels se manifestent ou s’aggravent souvent en présence de stress aigus ou continus provenant de la vie quotidienne. De plus, il importe de souligner que les personnes ayant subi un choc traumatique dans l’enfance paraissent sensibles aux effets néfastes de facteurs de stress ultérieurs sur la santé.3,4 Il semble que les expériences négatives vécues à l’étape du développement rendent vulnérable aux répercussions du stress plus tard dans la vie et prédisposent aux troubles liés à celui-ci.
Sujet
Le mécanisme précis par lequel l’adversité dans les jeunes années influe sur la vulnérabilité au stress et la prédisposition à la maladie plus tard dans la vie a fait l’objet de recherches intensives en neuroscience. Dans des études réalisées sur des rongeurs et des primates autres que l’être humain, des chercheurs ont examiné les effets des expériences des premières années de vie sur la structure et la fonction du cerveau, notamment en ce qui concerne le génome, et sur la modification de la sensibilité au stress qui peut s’ensuivre. Les résultats de ces travaux semblent indiquer que des expériences négatives, comme la séparation d’avec la mère ou des soins maternels insuffisantes, produisent des changements persistants sur les circuits neuraux qui interviennent dans l’intégration des processus de traitement cognitif et émotionnel, qui contrôlent l’axe hormonal du stress ainsi que le système nerveux autonome et qui régissent l’éveil et la vigilance. Ces changements intensifient la réaction physiologique aux facteurs de stress ultérieurs, de même que les comportements assimilables à la dépression, l’anxiété, la déficience cognitive, la sensibilité à la douleur et l’altération du sommeil.5,6 Il est concevable qu’une expérience négative dans l’enfance puisse avoir un lien de cause à effet avec divers troubles émotifs et physiques, particulièrement devant une difficulté.
Problème
On ne sait pas vraiment si les conclusions des travaux portant sur les effets neurobiologiques d’un stress précoce observés sur des sujets animaux peuvent être appliquées aux humains ni dans quelle mesure ces effets peuvent contribuer à l’apparition de troubles liés au stress précoce dans les études épidémiologiques.
Questionclé pour la recherche
Dans la recherche clinique, il importe de se pencher sur la question fondamentale suivante : les expériences négatives dans l’enfance sont-elles associées à des changements neurobiologiques semblables à ceux observés chez les animaux, et les modifications ainsi opérées ont-elles un lien avec des troubles comme la dépression majeure?
Contexte de la recherche
On a tenté, en menant des études cliniques ces dernières années, de mettre en lumière les mécanismes qui relient les traumatismes dans l’enfance aux risques de maladie à l’âge adulte. La recherche a porté en premier lieu sur l'axe corticotrope ou axe hypotalamo-hypophyso-surrénalien (axe HHS), qui est le principal système hormonal régulant la réponse de l’organisme au stress. Au niveau du cerveau, une hormone appelée corticolibérine (CRH) stimule l’axe HHS et amène la glande surrénale à sécréter le cortisol, c’est-à-dire l’hormone du stress. Le cortisol exerce sur le métabolisme, le comportement et le système immunitaire une action multiple qui aide l’organisme à s’adapter aux situations difficiles. Plusieurs régions du cerveau modulent l’axe HHS. Celles qui ont sur lui un effet inhibiteur sont l’hippocampe et le cortex préfrontal. L’amygdale et les fibres noradrénergiques du tronc cérébral activent la réaction au stress. Le cortisol, de son côté, ferme l’axe HHS dans plusieurs zones du cerveau. Une exposition soutenue ou accrue aux glucocorticoïdes peut avoir des effets néfastes sur l’hippocampe, ce qui entraîne une diminution des synapses et de la production de neurones. Une surexposition au cortisol nuit également au cortex préfrontal. Un tel dommage pourrait réduire peu à peu le contrôle de l’axe HHS et faire augmenter les réactions au stress7-8.
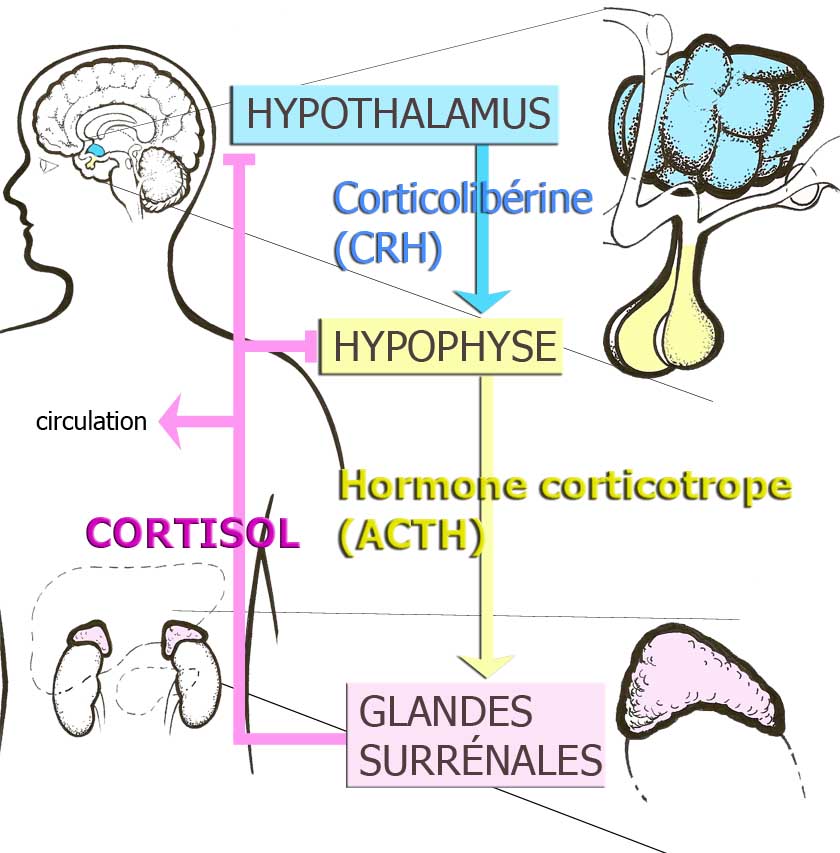
Figure 1. Axe hypothalamo-hypophyso-surrénalien (axe HHS) ou Axe hormonal du stress
Les neurones CRH intègrent également l’information pertinente au stress dans plusieurs régions du cerveau extérieures à l’hypothalamus. L’administration directe de CRH dans le cerveau des animaux produit une réaction endocrine, autonome et comportementale qui correspond aux signes du stress, de la dépression et de l’anxiété. La CRH et un autre neurotransmetteur, la noradrénaline, interagissent dans un circuit qui relie l’amygdale et l’hypothalamus à la région du tronc cérébral appelée locus coeruleus, pour assurer la régulation de la vigilance, de l’anxiété et de la peur et intégrer les réactions endocrines et autonomes.9-10
Toute perturbation de ces systèmes à la suite d’un stress précoce pourrait vraisemblablement conduire à une modification de la réactivité au stress et entraîner les changements émotifs, cognitifs et physiques caractéristiques des troubles liés au stress.
Résultats de la recherche
Les principales conclusions d’études cliniques rétrospectives chez des humains adultes ayant subi un traumatisme dans l’enfance sont les suivantes :
- Les femmes qui ont été victimes de mauvais traitements dans leurs premières années de vie affichent, par rapport aux sujets témoins, une augmentation marquée de l’hormone du stress et du rythme cardiaque lorsqu’elles sont soumises en laboratoire à un stress psychosocial qui consiste à parler en public et à effectuer des opérations de calcul mental. L’accroissement est particulièrement prononcé chez celles qui sont, en plus, dans un état dépressif.11 Des résultats semblables ont été rapportés chez les adultes ayant perdu un parent dans leur enfance,12 ce qui permet de croire que les résultats peuvent être appliqués à d’autres formes de stress précoce.
- Chez certaines femmes victimes de mauvais traitements, en particulier chez celles qui ne sont pas en dépression, la sécrétion de cortisol au repos est relativement réduite,13 bien que les conclusions à cet égard ne soient pas uniformes. Lorsque survient une situation perturbante, le manque de disponibilité de cortisol peut stimuler l’activation des systèmes cérébraux qui régissent la réaction au stress, entraînant une réactivité accrue au stress ainsi que des changements de comportement.
- La résistance relative de régions du cerveau au cortisol peut également contribuer à l’absence des effets régulateurs du cortisol, lequel agit par l’intermédiaire de récepteurs spéciaux qui peuvent diminuer en nombre ou devenir insensibles. Le test à la dexaméthasone/CRH peut être utilisé pour vérifier cette hypothèse. La dexaméthasone est une hormone glucocorticoïde de synthèse qui supprime l’action de l’axe HHS. Une injection subséquente de CRH provoque une augmentation du cortisol qui annule cet effet chez certaines personnes. C’est ce qu’on appelle un échappement, ce phénomène étant le marqueur le plus sensible de l’hyperactivité de l’axe HHS dans un état dépressif. Récemment, les traumatismes dans l’enfance ont été reliés à un échappement marqué à la suppression par la dexaméthasone chez les hommes adultes, particulièrement chez ceux qui souffrent de dépression, ce qui semble indiquer une diminution de la sensibilité aux rétroactions du cortisol dans des conditions stimulées.14
-
Une réactivité accrue du système nerveux autonome au stress associée à une altération de la sensibilité au cortisol pourrait augmenter l’activation immunitaire après un choc traumatique dans les premières années de vie. Ainsi, les hommes souffrant de dépression et ayant subi des traumatismes sérieux quand ils étaient enfants présentent une activation immunitaire accrue en réaction au stress psychosocial selon les mesures obtenues au moyen des marqueurs inflammatoires.15 L’augmentation de ces derniers a également été reliée à l’adversité dans l’enfance dans une récente étude prospective de cohortes.16 Les messagers du système immunitaire, comme les cytokines, peuvent stimuler encore les systèmes centraux de la CRH et accentuer le risque de plusieurs pathologies, dont la maladie cardiovasculaire et la fatigue chronique.
- Les conclusions qui précèdent correspondent à une activité accrue des systèmes centraux de la CRH. C’est pourquoi on a été constaté que les taux de CRH dans le liquide entourant le cerveau sont liés à un stress et à des expériences de mauvais traitement perçus dans l’enfance.2,17
- Comme il a été mentionné plus haut, l’hippocampe est une des régions les plus plastiques du cerveau qui agit comme catalyseur de la mémoire et du conditionnement au contexte. La séparation d’avec la mère et des injections de CRH pendant le développement modifient la structure et la plasticité de l’hippocampe chez les animaux de laboratoire. Un hippocampe plus petit que la normale est une caractéristique fondamentale de la dépression. Les traumatismes dans l’enfance ont été associés à des hippocampes de petite taille dans plusieurs études.18-20 Un lien a en outre été établi entre les traumatismes dans l’enfance et la petite taille de l’hippocampe chez les personnes en dépression.21 Des poussées répétées de CRH durant le développement ou une réactivité accrue au cortisol avec le temps peuvent contribuer à la taille réduite de l’hippocampe après un choc traumatique dans les premières années de vie et conduire à une plus grande sensibilité au stress.
-
Ce ne sont pas tous les sujets exposés à un traumatisme dans l’enfance qui présenteront un trouble, même soumis à des difficultés ultérieures. Pour comprendre le risque par opposition à la résilience, on peut, par exemple, considérer les interactions entre le stress précoce et les facteurs dispositionnels, comme les variations génétiques dans les systèmes neurobiologiques de réaction au stress. Par exemple, des effets modérateurs ont été constatés pour des variations de gènes dans divers systèmes cérébraux, y compris le système CRH et la sérotonine.22-25 Ces interactions gènes-environnement semblent refléter la modération génétique de la réponse fonctionnelle du cerveau au stress.
Lacunes de la recherche
Les travaux futurs devraient tenter de jeter la lumière sur le fondement neural et moléculaire de l’augmentation du risque après un choc traumatique dans l’enfance et intégrer ces mécanismes aux découvertes sur les hormones et aux symptômes cliniques. Des études recourant à l’imagerie fonctionnelle sont nécessaires pour établir des modèles de systèmes neuraux révélant une inadaptation au stress à la suite d’expériences malheureuses dans l’enfance. Il y aurait lieu d’examiner comment les dispositions génétiques, le sexe et les facteurs environnementaux interagissent pour provoquer des modifications du cerveau. L’accent devrait être mis en particulier sur les répercussions différentes de divers types de traumatismes à des étapes distinctes du développement afin que soient cernées les sources de la variabilité des résultats. Une telle recherche peut faire ressortir les marqueurs biologiques du risque et permettre l’établissement de cibles précises ainsi que la détermination de périodes propices pour la prévention de résultats négatifs. Pour atteindre cet objectif et décrire les trajectoires développementales de tels résultats par opposition à la résilience, il faudra procéder à des études longitudinales.
Conclusions et implications
En conclusion, les résultats d’études cliniques laissent entendre que le stress précoce chez les humains est associé à des changements neurobiologiques à long terme comparables à ceux qui sont décrits dans les études sur les animaux et semblent indiquer une sensibilisation au stress. Les variations génétiques des systèmes de réaction au stress atténuent le lien entre les traumatismes dans l’enfance et les réactions négatives. Il importe de souligner que dans les études susmentionnées, les modifications des systèmes de réaction au stress n’ont été constatées que chez les personnes ayant subi un choc traumatique dans l’enfance et souffrant de dépression mais non chez les personnes atteintes de dépression n’ayant pas connu de stress précoce important. Regroupés, ces résultats signifient que plusieurs des caractéristiques classiques de la dépression peuvent découler d’un stress précoce et manifester une prédisposition à la dépression et probablement à d’autres troubles devant une difficulté. Ils laissent aussi entendre qu’il peut exister des sous-types biologiquement discernables de dépression et d’autres désordres fonctionnels résultant d’un traumatisme dans l’enfance. Cette thèse est également appuyée par les conclusions de travaux réalisés sur la différence de sensibilité à la psychothérapie et à la pharmacothérapie chez les personnes atteintes de dépression chronique selon qu’elles ont subi ou non un traumatisme dans leurs premières années de vie26 et chez celles qui souffrent du syndrome du côlon irritable.27 Ainsi, l’examen des facteurs développementaux peut aider à améliorer la classification diagnostique des troubles somatiques mentaux et fonctionnels et, ultimement, à éclairer les décisions concernant le traitement à adopter.
Références:
- Margolin G, Gordis EB. The effects of family and community violence on children. Annual Review of Psychology 2000; 51:445-479.
- Anda RF, Felitti VJ, Bremner JD, Walker JD, Whitfield C, Perry BD, Dube SR, Giles WH. The enduring effects of abuse and related adverse experiences in childhood. A convergence of evidence from neurobiology and epidemiology. European Archives of Psychiatry and Clinical Neuroscience 2006:256(3):174-186.
- Dougherty LR, Klein DN, Davila J. A growth curve analysis of the course of dysthymic disorder: the effects of chronic stress and moderation by adverse parent-child relationships and family history. Journal of Consulting and Clinical Psychology 2004; 72(6):1012-1021.
- Kendler KS, Kuhn JW, Prescott CA. Childhood sexual abuse, stressful life events and risk for major depression in women. Psychological Medicine 2004; 34:1475-1482.
- Ladd CO, Huot RL, Thrivikraman KV, Nemeroff CB, Meaney MJ, Plotsky PM. Long-term behavioral and neuroendocrine adaptations to adverse early experience. Progress in Brain Research 2000;122:81-103.
- Meaney MJ, Szyf M. Environmental programming of stress responses through DNA methylation: life at the interface between a dynamic environment and a fixed genome. Dialogues in Clinical Neuroscience 2005;7(2):103-123.
- Arborelius L, Owens MJ, Plotsky PM, Nemeroff CB. The role of corticotropin-releasing factor in depression and anxiety disorders. Journal of Endocrinology 1999;160(1):1-12.
- Fuchs E, Gould E. Mini-review: in vivo neurogenesis in the adult brain: regulation and functional implications. European Journal of Neuroscience 2000;12(7):2211-2214.
- Owens MJ, Nemeroff CB. Physiology and pharmacology of corticotropin-releasing factor. Pharmacological Review 1991;43(4):425-473.
- Koob GF. Corticotropin-releasing factor, norepinephrine, and stress. Biological Psychiatry 1999;46(9):1167-1180.
- Heim C, Newport DJ, Heit S, Graham YP, Wilcox M, Bonsall R, Miller AH, Nemeroff CB. Pituitary-adrenal and autonomic responses to stress in women after sexual and physical abuse in childhood. JAMA – Journal of the American Medical Association 2000;284(5): 592-597.
- Luecken LJ. Childhood attachment and loss experiences affect adult cardiovascular and cortisol function. Psychosomatic Medicine 1998;60(6):765-772
- Heim C, Newport DJ, Bonsall R, Miller AH, Nemeroff CB. Altered pituitary-adrenal axis responses to provocative challenge tests in adult survivors of childhood abuse. American Journal of Psychiatry 2001;158(4):575-581.
- Heim C, Mletzko T, Purselle D, Musselman DL, Nemeroff CB. The dexamethasone/corticotropin-releasing factor test in men with major depression: role of childhood trauma. Biological Psychiatry 2008;63(4):398-405.
- Pace TWW, Mletzko T, Alagbe O, Musselman DL, Nemeroff CB, Miller AH, Heim C. Increased stress-induced inflammatory responses in male patients with major depression and increased early life stress. American Journal of Psychiatry 2006;163(9):1630-1633.
- Danese A., Pariante CM, Caspi A, Taylor A, Poulton R. Childhood maltreatment predicts adult inflammation in a life-course study. Proceedings of the National Academy of Sciences of the United States of America 2007;104(4):1319-1324.
- Carpenter LL, Tyrka AR, McDougle CJ, Malison RT, Owens MJ, Nemeroff CB, Price LH. Cerebrospinal fluid corticotropin-releasing factor and perceived early-life stress in depressed patients and healthy control subjects. Neuropsychopharmacology 2004;29(4):777-784.
- Bremner JD, Randall P, Vermetten E, Staib L, Bronen RA, Mazure C, Capelli S, McCarthy G, Innis RB, Charney DS. Magnetic resonance imaging-based measurement of hippocampal volume in posttraumatic stress disorder related to childhood physical and sexual abuse--a preliminary report. Biological Psychiatry 1997;41(1): 23-32.
- Stein MB, Koverola C, Hanna C, Torchia MG, McClarty B, Hippocampal volume in women victimized by childhood sexual abuse. Psychological Medicine 1997; 27(4):951-959.
- Driessen M, Herrmann J, Stahl K, Zwaan M, Meier S, Hill A, Osterheider M, Petersen D. Magnetic resonance imaging volumes of the hippocampus and the amygdala in women with borderline personality disorder and early traumatization. Archives of General Psychiatry 2000; 57(12):1115-1122.
- Vythilingam M, Heim C, Newport DJ, Miller,AH, Vermetten E, Anderson E, Bronen R, Staib L, Charney DS, Nemeroff CB, Bremner JD. Childhood trauma associated with smaller hippocampal volume in women with major depression. American Journal of Psychiatry 2002;159(12):2072-2080.
- Caspi A, Sugden K, Moffitt TE, Taylor A, Craig IW, Harrington H, McClay J, Mill J, Martin J, Braithwaite A, Poulton R. Influence of life stress on depression: moderation by a polymorphism in the 5-HTT gene. Science 2003;301(5631):386-389.
- Kendler KS, Kuhn JW, Vittum J, Prescott CA, Riley B. The interaction of stressful life events and a serotonin transporter polymorphism in the prediction of episodes of major depression: a replication. Archives of General Psychiatry 2005. 62(5):529-535.
- Kaufman J, Yang BZ, Douglas-Palumberi H, Houshyar S, Lipschitz D, Krystal JH, Gelernter J. 2004. Social supports and serotonin transporter gene moderate depression in maltreated children. Proceedings of the National Academy of Sciences USA 2004;101(49):17316-1721.
- Bradley RG, Binder EB, Epstein M, Tang Y, Nair H, Liu W, Gillespie CF, Berg T, Evces M, Heim CM, Nemeroff CB, Schwartz A, Cubells JF, Ressler KJ. Influence of child abuse on adult depression: moderation by the corticotropin-releasing hormone receptor gene. Archives of General Psychiatry 2008; 65(2):190-200.
- Nemeroff CB, Heim C, Thase ME, Rush AJ, Schatzberg AF, Ninan PT, Klein DN, McCullough JP, Weiss P, Dunner DL, Rothbaum BO, Kornstein S, Keitner G, Keller MB. Differential responses to psychotherapy versus pharmacotherapy in the treatment of patients with chronic forms of major depression and childhood trauma. Proceedings of the National Academy of Sciences USA 2003. 100(24):14293-14296.
- Creed F, Guthrie E, Ratcliffe J, Fernandes L, Rigby C, Tomenson B, Read N, Thompson DG. Reported sexual abuse predicts impaired functioning but a good response to psychological treatments in patients with severe irritable bowel syndrome. Psychosomatic Medicine 2005; 67:490-499.
Pour citer cet article :
Heim C. Traumatisme dans l’enfance et sensibilité au stress à l’âge adulte. Dans: Tremblay RE, Boivin M, Peters RDeV, eds. Encyclopédie sur le développement des jeunes enfants [en ligne]. https://www.enfant-encyclopedie.com/cerveau/selon-experts/traumatisme-dans-lenfance-et-sensibilite-au-stress-lage-adulte. Publié : Août 2009. Consulté le 16 mai 2026.
Texte copié dans le presse-papier ✓